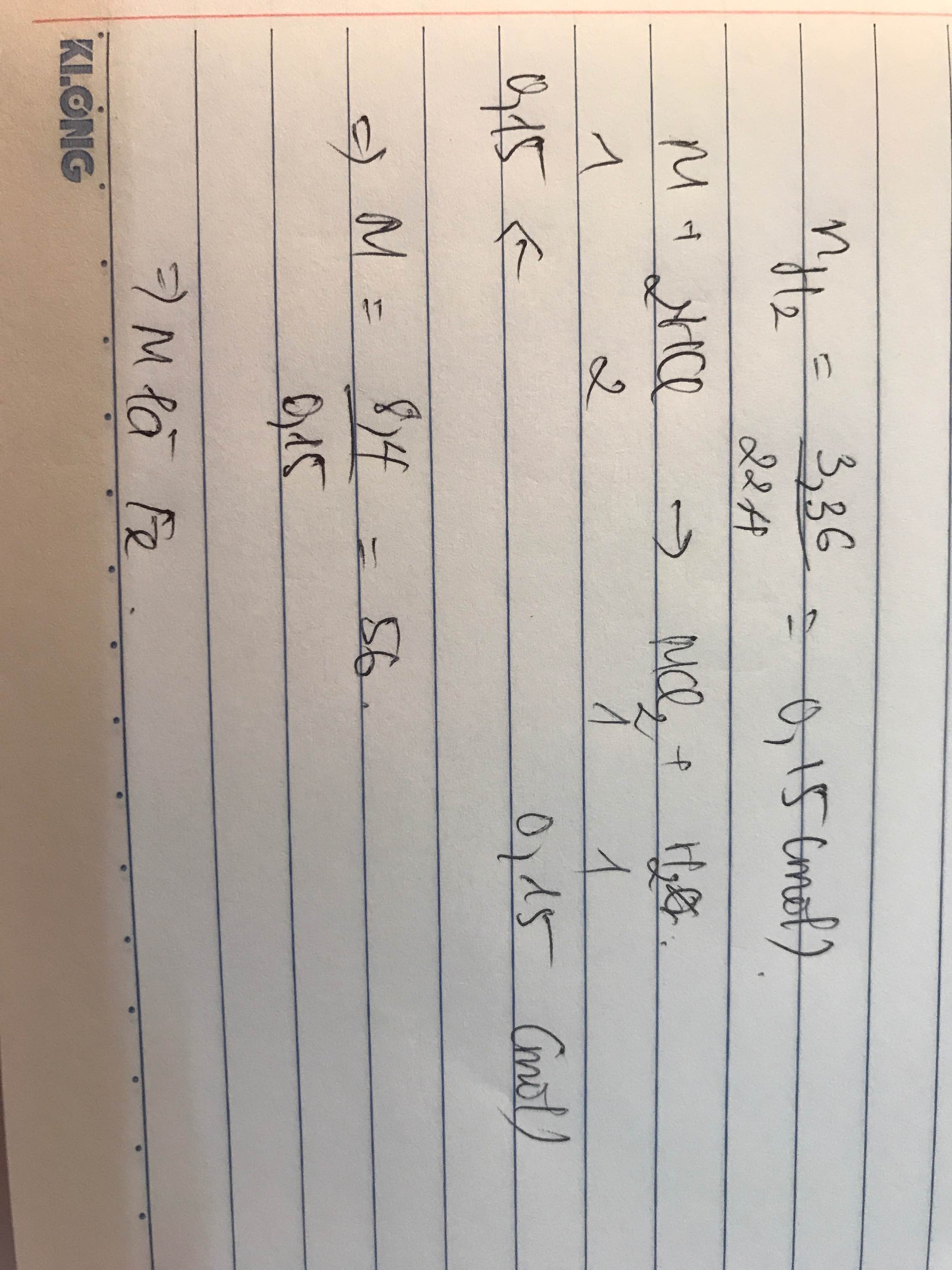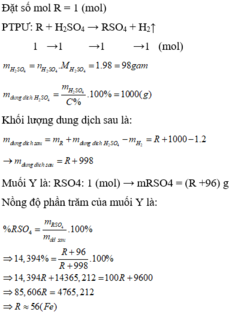Những câu hỏi liên quan
cho 8,4 gam một kim loại M hóa trị II vào dung dịch HCl 10% dư. Sau khi kim loại hòa tan hoàn toàn thu được 3,36 lít khí đo ở đktc và dung dịch A.
a. Xác định kim loại M
b.Để phản ứng hết dung dịch A cần 500ml dung dịch NaOH 1M. Tính nồng độ phần trăm các chất trong dung dịch A
dạ em làm xong câu B rồi mọi người khỏi cần trả lời nữa ạ
Đúng 0
Bình luận (2)
Hòa tan 14,4 gam kim loại R hóa trị II trong dung dịch HCl 29,2%. Sau khi phản ứng hoàn toàn thu được dung dịch mới có nồng độ HCl 5,456% và nồng độ muối clorua là 28,401%. Xác định kim loại R.
Câu 8: Cho 8,3g hỗn hợp X gồm Fe và Al vào 1lít dung dịch CuSO4 0,2 M, sau khi phản ứng xảy ra hoàn toàn thu được 15,68g chất rắn Y gồm 2 kim loại.
a) Tính thành phần phần trăm theo khối lượng của từng kim loại trong hỗn hợp X.
b) Tính nồng độ mol/l của các chất tan trong dung dịch sau phản ứng.
c) Trình bày phương pháp hoá học để tách riêng từng kim loại trong Y.
a, 2Al + 3CuSO4 → Al2(SO4)3 + 3Cu
x…………3/2.x
Fe + CuSO4 → FeSO4 + Cu
y……..y
Al phản ứng hết với CuSO4 sau đó Fe mới phản ứng với CuSO4. Vì sau phản ứng thu được rắn Y gồm 2 kim loại nên Al đã tan hết và Fe có thể đã phản ứng 1 phần hoặc chưa phản ứng. 2 kim loại trong Y là Fe và Cu.
⇒ nCu = nCuSO4 = 0,2.1 = 0,2 mol
⇒ mFe dư = mY - mCu = 15,68 - 0,2.64 = 2,88g
Đặt số mol Al ban đầu là x, số mol Fe phản ứng là y, ta có hệ phương trình:
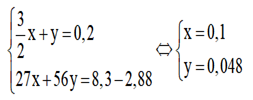
⇒ mAl = 0,1.27 = 2,7g
⇒ %mAl = 2,7/8,3.100 = 32,53%
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn 14,2g hỗn hợp C gồm MgCO3, muối CO3 của kim loại R vào axit HCl 7,3 phần trăm vừa đủ thu được dung dịch D và 3,36l khí CO2( đktc). Nồng độ MgCl2 trong dung dịch D 6,028 phần trăma) Xác định kim loại R và thành phần phần trăm theo khối lượng trong Cb) Cho NaOH dư vào D, lọc lấy kết tủa rồi nung ngoài không khí đến khi phản ứng xảy ra hoàn toàn. Tính khối lượng chất dằn còn lại sau khi nung
Đọc tiếp
Hòa tan hoàn toàn 14,2g hỗn hợp C gồm MgCO3, muối CO3 của kim loại R vào axit HCl 7,3 phần trăm vừa đủ thu được dung dịch D và 3,36l khí CO2( đktc). Nồng độ MgCl2 trong dung dịch D = 6,028 phần trăm
a) Xác định kim loại R và thành phần phần trăm theo khối lượng trong C
b) Cho NaOH dư vào D, lọc lấy kết tủa rồi nung ngoài không khí đến khi phản ứng xảy ra hoàn toàn. Tính khối lượng chất dằn còn lại sau khi nung
Gọi: M là NTK của R
a là số oxi hóa của R trong muối --> CTPT muối của R là R(2/a)CO3.
a) Từ nCO2 = n hỗn hợp = 0,5 nHCl = 3,36/22,4 = 0,15
--> nHCl = 0,15 x 2 = 0,3 mol nặng 0,3 x 36,5 = 10,95 gam.
--> dung dịch axit HCl 7,3% nặng 10,95/0,073 = 150 gam.
Mà
m dung dịch sau phản ứng = m dung dịch axit + m C - m CO2 bay ra
= 150 + 14,2 - (0,15 x 44) = 157,6 gam
--> m MgCl2 = 0,06028 x 157,6 = 9,5 gam
--> n MgCl2 = 9,5/95 = 0,1 mol = n MgCO3
--> m MgCO3 = 0,1 x 84 = 8,4 gam chiếm 8,4/14,2 = 59,154929%
--> m R(2/a)CO3 = 14,2 - 8,4 = 5,8 gam chiếm 5,8/14,2 = 40,845071%
--> n R(2/a)CO3 = 0,15 - 0,1 = 0,05 mol.
--> PTK của R(2/a)CO3 = 5,8/0,05 = 116.
--> 2M/a = 116 - 60 = 56 hay M = 23a.
Chọn a = 2 với M = 56 --> R là Fe.
b) Khối lượng chất rắn sau khi nung đến khối lượng không đổi là khối lượng của 0,1 mol MgO và 0,05 mol FeO(1,5). (FeO(1,5) là cách viết khác của Fe2O3. Cũng là oxit sắt 3 nhưng PTK chỉ bằng 80).
m chất rắn sau khi nung = (0,1 x 40) + (0,05 x 80) = 8 gam.
Đúng 0
Bình luận (1)
Cho 9,2 gam hỗn hợp kim loại Mg và Fe vào 210 ml dung dịch CuSO4 1M. Sau khi phản ứng xảy ra hoàn toàn thu được dung dịch X và 15,68 gam hai kim loại. Phần trăm khối lượng của Fe trong hỗn hợp ban đầu là A .60,87% B .24,35% C .36,52% D .70,43%
Đọc tiếp
Cho 9,2 gam hỗn hợp kim loại Mg và Fe vào 210 ml dung dịch CuSO4 1M. Sau khi phản ứng xảy ra hoàn toàn thu được dung dịch X và 15,68 gam hai kim loại. Phần trăm khối lượng của Fe trong hỗn hợp ban đầu là
A .60,87%
B .24,35%
C .36,52%
D .70,43%
nCu=0.21 nMg=a,nFe=b
24a+56b=9.2
a*(64-24)+(0.21-a)*(064-56)=15.68-9.2 nên a=0.15 b=0.1
%fe=60.8%
Đáp án A
Đúng 0
Bình luận (0)
Ngâm bột kẽm trong 80 gam dung dịch muối CuSO4 30%. Sau khi phản ứng xảy ra hoàn toàn, thu được dung dịch và 16,1 gam hỗn hợp kim loại A. Tính khối lượng kẽm đã phản ứng và nồng độ phần trăm chất tan trong dung dịch thu được
Sau phản ứng, thu được hỗn hợp kim loại, suy ra kẽm dư.
$n_{CuSO_4} = \dfrac{80.30\%}{160} = 0,15(mol)$
$Zn + CuSO_4 \to ZnSO_4 + Cu$
$n_{Zn\ pư} = n_{CuSO_4} = 0,15(mol)$
$\Rightarrow m_{Zn\ pư} = 0,15.65 = 9,75(gam)$
Sau phản ứng, $m_{dd} = 9,75 + 80 - 0,15.64 = 80,15(gam)$
$C\%_{ZnSO_4} = \dfrac{0,15.161}{80,15}.100\% = 30,13\%$
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn một kim loại R có hóa trị II bằng dung dịch
H
2
SO
4
9,8% (loãng) vừa đủ, sau phản ứng thu được dung dịch X chứa muối Y với nồng độ phần trăm là 14,394%. Kim loại R là: A. Mg. B. Fe. C. Zn. D. Cu.
Đọc tiếp
Hòa tan hoàn toàn một kim loại R có hóa trị II bằng dung dịch H 2 SO 4 9,8% (loãng) vừa đủ, sau phản ứng thu được dung dịch X chứa muối Y với nồng độ phần trăm là 14,394%. Kim loại R là:
A. Mg.
B. Fe.
C. Zn.
D. Cu.
Hỗn hợp rắn X gồm M, MO và MCl2 (M là kim loại có hóa trị II không đổi). Cho 18,7 gam X tác dụng với dung dịch HCl (vừa đủ), thu được dung dịch A và 6,72 lít khí (đktc). Cho dung dịch NaOH dư vào dung dịch A, sau phản ứng thu được kết tủa B. Nung B ở nhiệt độ cao đến khối lượng không đổi thu được 18,0 gam chất rắn. Mặt khác, khi cho 18,7 gam hỗn hợp X vào 500 ml dung dịch CuCl2 1,0M, sau phản ứng, tách bỏ chất rắn rồi cô cạn dung dịch, thu được 65,0 gam muối khan. Biết các phản ứng hóa học xảy r...
Đọc tiếp
Hỗn hợp rắn X gồm M, MO và MCl2 (M là kim loại có hóa trị II không đổi). Cho 18,7 gam X tác dụng với dung dịch HCl (vừa đủ), thu được dung dịch A và 6,72 lít khí (đktc). Cho dung dịch NaOH dư vào dung dịch A, sau phản ứng thu được kết tủa B. Nung B ở nhiệt độ cao đến khối lượng không đổi thu được 18,0 gam chất rắn. Mặt khác, khi cho 18,7 gam hỗn hợp X vào 500 ml dung dịch CuCl2 1,0M, sau phản ứng, tách bỏ chất rắn rồi cô cạn dung dịch, thu được 65,0 gam muối khan. Biết các phản ứng hóa học xảy ra hoàn toàn.
Xác định kim loại M và tính thành phần phần trăm theo khối lượng của các chất có trong hỗn hợp X.
Nhiệt phân hoàn toàn 7,26 gam muối nitrat của kim loại R hóa trị III, sau phản ứng thu được 2,4 gam oxit kim loại và hỗn hợp khí A.
a) Xác định kim loại R.
b) Hấp thụ toàn bộ khí A vào 100 ml H2O thu được dung dịch B. Tính pH của dung dịch B ?